Vertaling van enkele web-artikelen en van een artikel uit een medisch tijdschrift over hoe het virus het lichaam binnendringt en de auto-immuunziekten veroorzaakt.
https://www.verywellhealth.com/is-epstein-barr-linked-to-autoimmune-disease-4165847 en
https://www.palomahealth.com/learn/epstein-barr-virus-thyroid
Het Epstein-Barr-virus (EBV) is een type herpesvirus. Het komt zeer vaak voor. Het kan mononucleosis veroorzaken, ook bekend als mono of ziekte van Pfeiffer.Volgens een onderzoek uit 2018 (https://pubmed.ncbi.nlm.nih.gov/29662164/) kan (EBV) het risico op het ontwikkelen van een auto-immuunziekte verhogen. Onderzoekers zeggen dat het virus bepaalde genen lijkt “aan te zetten”. Deze genen maken je meer kans om een van deze aandoeningen te ontwikkelen.
Wetenschappers zijn al lang op de hoogte van het verband tussen EBV en sommige auto-immuunziekten. Dit is echter de eerste studie die al deze ziekten in verband brengt met EBV. Het is ook de eerste die een verklaring geeft voor het hoe en waarom van dit verband.
Het Epstein-Barr virus is een van de meest voorkomende virussen die mensen infecteren. Bijna iedereen draagt het bij zich.Je hoort het vaakst over EBV als de oorzaak van infectieuze mononucleose. Deze ziekte wordt ook wel Pfeiffer of de “kissing disease” genoemd.
EBV is een lid van de herpesvirus familie. Net als andere virussen in deze groep, blijf je drager van het virus als je het eenmaal hebt.
EBV blijft meestal sluimeren. Als het toch weer actief wordt, kan een gezond immuunsysteem het gemakkelijk weer in een slapende toestand brengen.
Bij sommige mensen kan de eerste infectie echter langdurige problemen veroorzaken. De infectie kan genen activeren die van invloed zijn op de werking van het immuunsysteem. Dit is slechts één van de mogelijke lange termijn effecten van EBV.
Wat is een auto-immuunziekte?
Uw immuunsysteem zendt speciale cellen uit om gevaarlijke dingen te doden. Dit omvat indringers zoals virussen en bacteriën.
Auto-immuniteit is als een geval van persoonsverwisseling. Uw immuunsysteem richt zich ten onrechte op dingen die in uw lichaam horen te zitten, zoals een orgaan of weefseltype.
Dit leidt tot ontsteking en weefselbeschadiging. Mensen met deze aandoeningen kunnen pijn ervaren. Ze kunnen ook vreselijk vermoeid zijn.. Dit gebeurt omdat het lichaam middelen aanwendt voor de immuunreactie.
Andere symptomen hangen af van wat er beschadigd is. Bijvoorbeeld, uw alvleesklier produceert insuline. Insuline helpt uw lichaam suikers te verwerken. Als uw immuunsysteem uw alvleesklier aanvalt, zult u problemen hebben met het verwerken van suikers.
Voorbestemdheid en genetische verwisseling
De meesten van ons denken dat genetica vastligt. Zo eenvoudig ligt het echter niet. Ziekte, omgeving en andere variabelen kunnen genen in- of uitschakelen.
Denk aan een stroomonderbreker. Als je een schakelaar uitzet, verlies je stroom in een deel van je huis. Zet je hem aan, komt de stroom er weer op. Hetzelfde gebeurt met genen en hun positieve of negatieve effect op het lichaam.
Veel mensen worden geboren met genetische aanleg voor bepaalde ziekten. Dit betekent niet dat ze deze ziekten zullen ontwikkelen. Ze kunnen ze wel krijgen onder de juiste omstandigheden.
Hoe het Epstein-Barr Virus het immuunsysteem bedriegt
De studie van 2018 toonde aan dat EBV in staat lijkt te zijn om de genen in te schakelen die auto-immuunziekten veroorzaken. Iemand zonder genetische aanleg kan echter EBV oplopen zonder dat dit gebeurt.
Onderzoekers keken naar de genetische impact van verschillende eiwitten in EBV. Zij ontdekten dat een eiwit, Epstein-Barr virus nucleair antigeen 2 (EBNA2) genaamd, interageert met de helft van de bekende genen die een persoon een risico op lupus geven.
Verband tussen Epstein-Barr virus en auto-immuunziekte van de schildklier
EBV is een bekende uitlokkende factor voor een aantal auto-immuunziekten. Een eiwit dat Epstein-Barr produceert, hecht zich aan locaties in het menselijk genoom die in verband worden gebracht met zeven auto-immuunziekten: multiple sclerose, reumatoïde artritis (RA), juveniele idiopathische artritis, systemische lupus erythematosus (SLE), inflammatoire darmziekte, coeliakie en type 1 diabetes.
Onderzoekers in Polen hebben ook een zeer hoge prevalentie van EBV-infectie gevonden bij zowel patiënten met thyreoditis van Hashimoto als patiënten met de ziekte van Graves in vergelijking met de algemene bevolking. De ziekten van Hashimoto en Graves zijn de twee meest voorkomende auto-immuunziekten. Ze treffen naar schatting tot 10 procent van de mensen wereldwijd.
Uit de Poolse studie bleek dat bij 81 procent van de gevallen van thyreoïditis van Hashimoto en bij 63 procent van de gevallen van de ziekte van Graves EBV-eiwitten in de schildklier aantoonbaar waren. Deze bevindingen suggereren dat chronische EBV en EBV-herinfectie auto-immuun schildklierziekten kunnen veroorzaken.
Deskundigen schrijven 60 tot 70 procent van auto-immuun schildklieraandoeningen toe aan uw genetica. Genetica en familiegeschiedenis zijn echter maar een deel van het plaatje. Ook andere factoren spelen een rol, zoals blootstelling aan straling, een tekort aan selenium, een teveel aan jodium, fysieke of emotionele stress, voeding, zwangerschap, andere hormonale onevenwichtigheden, trauma aan de hals of de schildklier, roken, bacteriële en virale infecties en sommige medicijnen.
Hoewel dit nog in onderzoek is, is de theorie dat met EBV geïnfecteerde immuuncellen de schildklier infiltreren bij mensen die aanleg hebben voor auto-immuniteit, waaronder auto-immuunziekte van de schildklier. Als ze eenmaal voet aan de grond hebben gekregen in de schildklier, beginnen de met EBV geïnfecteerde cellen antilichamen te produceren en zorgen ze ervoor dat de omringende immuuncellen overreageren en de schildklier aanvallen.
Een gezond immuunsysteem stopt dit proces meestal snel. Maar bij iemand met een genetisch of door de omgeving aangetast immuunsysteem, grijpt het virus om zich heen. Herinfecties kunnen periodiek opflakkeren en niet alleen symptomatische EBV-herinfectie veroorzaken. Maar ze kunnen ook auto-immuniteit in de schildklier zelf “aanzetten”.
Maar laten we duidelijk zijn. U zult waarschijnlijk informatie tegenkomen van leunstoel “experts” en zogenaamde “medische mediums” die beweren dat EBV de oorzaak is van alle auto-immuun schildklierziekten en zelfs schildklierkanker. Dat is niet alleen onbewezen, maar ook hoogst onwaarschijnlijk.
Auto-immuunziekten zijn zeer complex en hebben meestal te maken met vele omgevingsfactoren en immuunfactoren. Alles, van h. pylori gastro-intestinale infecties tot glutengevoeligheid en onevenwichtige voeding, kan bijdragen aan het risico op het ontwikkelen van auto-immuun schildklierziekte.
Epstein–Barr Virus Reactivatie-geinduceeer Immunoglobuline Productie: de significantie voor auto-immuniteit
- B-cellen zijn lymfocyten die een belangrijke rol spelen in het immuunsysteem
- Plasmacellen zijn volledig geactiveerde B-cellen. Deze cellen produceren grotere hoeveelheden antilichamen tegen specifieke ziekteIgM
- Ig zijn immunoglobulinen, oftewel antistoffen
- IgM-= IgM is een type antilichaam dat wordt geproduceerd door B-cellen. Het is verreweg het grootste en zwaarste type antilichaam in de menselijke circulatie. Het is meestal het eerste antilichaam dat men in het bloed ziet verschijnen als respons op een antigeen
Samenvatting van het artikel :
https://www.mdpi.com/2076-2607/8/12/1875/htm
Het Epstein-Barr virus (EBV) houdt zich voornamelijk op in B-cellen, die differentiëren in antilichaam-producerende cellen, en dus is EBV betrokken bij auto-immuunziekten. Wij hebben getracht de her-activatie van EBV te beschrijven en de relevantie ervan voor auto-immuunziekten, met de nadruk op de ziekte van Graves, een auto-immuunziekte die hyperthyreoïdie veroorzaakt door TSH receptorantilichamen.
Circulerende autoreactieve B-cellen die aan de selectie zijn ontsnapt, vinden het moeilijk om de cellen te onderscheiden en antilichamen te produceren. Wanneer EBV dergelijke B-cellen echter infecteert en reactiveert, kunnen de B-cellen plasmacellen worden en autoantilichamen produceren.
Wij hebben hier een EBV reactivatie-geïnduceerd Ig produktiesysteem voorgesteld, dat een andere route volgt dan het antilichaam produktiesysteem via kiemcentra en beenmerg en de volgende kenmerken heeft:
1. IgM dominantie,
2. alomtegenwoordige Ig productie, en
3. de redding van auto-reactieve B-cellen, die de Ig productie scheeftrekt naar autoantigenen.
IgM-autoantilichamen die worden opgewekt door EBV-reactivatie kunnen de klassieke complementroute activeren en gezond weefsel beschadigen, dat autoantigenen levert voor de productie van affiniteit-gerijpte IgG-autoantilichamen. Antilichamen opgewekt door EBV reactivatie kunnen een belangrijke rol spelen in de ontwikkeling en verergering van auto-immuunziekten.
3. De ziekte van Graves is een auto-immuunziekte van de schildklier
In onze studie van EBV-reactivatie en auto-immuniteit hebben we de ziekte van Graves, een auto-immuunziekte van de schildklier dat zich uit in hyperthyreoïdie, als voorbeeld genomen, omdat het aantal patiënten met de ziekte van Graves groot is, en er dus veel efficiënte antilichamen of receptoreiwitten beschikbaar waren. De mechanismen die we hier aantonen kunnen gemeenschappelijk zijn in elke auto-immuunziekte, en daarom willen we graag uitleg geven over de EBV-reactivatie-opgewekte Ig productie en auto-immuniteit bij de ziekte van Graves.
De ziekte van Graves vertegenwoordigt de meerderheid van de gevallen van hyperthyreoïdie. Patiënten met de ziekte van Graves hebben een diffuus vergrote schildklier en verhoogde serum schildklierhormoonspiegels. Ze ontwikkelen hartkloppingen, ademnood (benauwdheid), warmte-intolerantie, of gewichtsverlies omdat schildklierhormoon het sympathische zenuwstelsel, de voedselvertering , en het metabolisme activeert.
[Elke cel in ons lichaam bevat receptorplaatsen voor schildklierhormonen. Schildklierhormonen zijn verantwoordelijk voor het meest elementaire en fundamentele aspect van onze fysiologie, metabolisme en meer. Onze schildklier is het centrum van onze cellulaire stofwisseling en is uiterst gevoelig voor kleine onevenwichtigheden in ons lichaam. Een disfunctie van de schildklier komt veel voor in onze samenleving en kan leiden tot functieverlies, neurologische symptomen en een vermindering van de levenskwaliteit.
De gezondheid van onze schildklier is uiterst gevoelig voor andere onevenwichtigheden in ons lichaam: andere soorten endocriene onevenwichtigheden, milieufactoren/toxinen, kruisreacties op medicijnen, en nog veel meer.
Het schildkliermetabolisme begint in onze hersenen! Om het proces van de aanmaak van schildklierhormoon te beginnen, produceert onze hypothalamus, thyrotropin releasing hormone (TRH). Dit gebied van onze hersenen (onze hypothalamus) wordt sterk beïnvloed door dopamine en serotonine neurotransmitters. Dat betekent dat elke factor die de aanmaak van deze zenders verstoort, invloed heeft op de schildklier. Dingen die een negatieve invloed hebben op de dopamine en serotonine in de hersenen zijn dieet, darmgezondheid, stress, slaap, beeldschermtijd en medicijnen.
Nadat TRH is vrijgegeven, wordt de hypofyse gestimuleerd. De hypofyse geeft dan schildklier-stimulerend hormoon (TSH) af. TSH dat in onze bloedstroom circuleert, zorgt ervoor dat onze cellen schildklierperoxidase (TPO) aanmaken. De schildklier produceert dan T4 en T3. Het grootste deel van de hormoonproductie in de schildklier is inactief T4. Ons lichaam kan T4 niet gebruiken, dus moet het T4 omzetten in T3 om nuttig te worden voor ons systeem.]
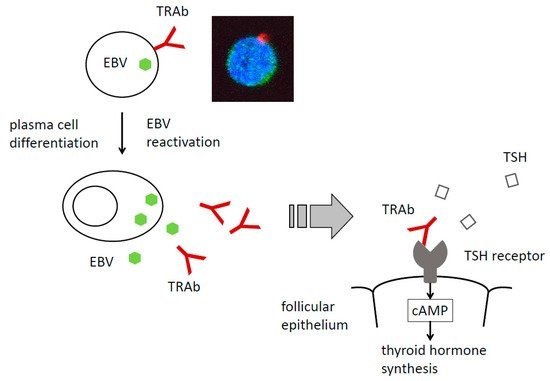
Thyrotropinereceptoren (TSHRs) op het oppervlak van het schildklierfollikel-epitheel binden thyrotropine (thyroïd-stimulerend hormoon: TSH) dat door de hypofyse wordt afgescheiden en signalen, waaronder cAMP voor de productie van schildklierhormoon, worden doorgegeven [33,34] (figuur 1). Patiënten met de ziekte van Graves hebben TSHR-autoantilichamen, TSI genaamd, die TSHR competitief binden met TSH. Hoewel de antistoffen van de ziekte van Graves uit 3 soorten bestaan, zijn de meeste van het stimulerende soort, hoewel er ook blokkerende antistoffen zijn.
Figuur 1. EBV reactivatie induceert plasma celdifferentiatie en de productie van thyrotropin receptor antilichamen (TRAbs). De reactivatie van EBV persisterend in TRAb-producerende cellen induceert plasmaceldifferentiatie en TRAb-productie. TRAb binden de thyrotropinereceptor (TSHR) competitief met thyrotropine (TSH) en stimuleren het schildklierfollikelepitheel. Inzet: Een TRAb (rood) en EBER1 (groen) dubbel-positieve cel.
Schildklieraandoeningen met lymfocytaire infiltratie van de schildklier en karakteristieke auto-antilichamen tegen schildkliercomponenten worden auto-immuun schildklieraandoeningen (AITD) genoemd. De ziekte van Graves en de thyreoïditis van Hashimoto zijn representatieve AITD, en TSI is het autoantilichaam voor de ziekte van Graves, terwijl het anti-thyroïde peroxidase (TPO-antistoffen) antilichaam en anti-thyroglobuline (Tg antistoffen) autoantilichamen zijn voor de thyreoïditis van Hashimoto. Een “gebeurtenis” dat tot een immuunrespons leidt, kan belangrijk zijn als mechanisme voor AITD.
De ziekte van Graves en de thyreoïditis van Hashimoto kunnen tegelijk voorkomen bij dezelfde patiënt en binnen dezelfde familie. Patiënten met de ziekte van Graves lopen een verhoogd risico op andere auto-immuunziekten, waaronder insuline-afhankelijke diabetes mellitus, myasthenia gravis, het syndroom van Sjögren en RA. Genetische factoren en omgevingsfactoren zijn voorgesteld als risicofactoren voor de ziekte van Graves. Een te lage jodiuminname, stress of infectie kunnen omgevingsfactoren zijn. De nadruk is echter gelegd op genetische (erfelijke) factoren, gebaseerd op eerdere bevindingen die aantoonden dat broers en zussen een hoog risico hadden om getroffen te worden en dat monozygote tweelingen een hoger concordantiepercentage hadden dan dizygote tweelingen [32,41,42].
Hoewel er tot op heden veel vatbare genen zijn gerapporteerd, waren hun risicoverhoudingen niet hoog: risicoverhoudingen van twee- tot viervoudig . Wij stelden hierin virale infecties voor als een belangrijke omgevingsfactor, namelijk Epstein-Barr virus (EBV) infectie.
9. Conclusies
Wij hebben hier een EBV reactivatie-geïnduceerd Ig productie systeem voorgesteld dat een alternatief systeem is voor antilichaam productie met de volgende kenmerken: IgM dominantie, ubiquitaire Ig productie, en de redding van autoreactieve B-cellen.
IgM-dominantie betekent dat door EBV-reactivatie geïnduceerde antilichamen doelwitcellen verwonden door activering van de klassieke complementroute. Alomtegenwoordige Ig-productie vereist geen kiemcentra of beenmerg. De redding van autoreactieve B-cellen die verwijderd moesten worden, resulteert in een scheve populatie voor auto-antilichamen, wat de reden kan zijn waarom verschillende auto-antilichamen verschijnen in IM, en de reden voor de overlapping van auto-immuunziekten.
Antilichamen geïnduceerd door EBV reactivatie kunnen een belangrijke rol spelen in de ontwikkeling en verergering van auto-immuunziekten. Het onderzoek naar EBV-reactivatie geïnduceerde Ig-productie is nog maar net begonnen. Verdere mechanismen zullen in de toekomst worden opgehelderd.
